 Fórum » CO2 » Zkušenosti a rady
Fórum » CO2 » Zkušenosti a rady
Flourish Exce, Easy Carbo a CO2 Vital
https://rybicky.net/vyrobky/1534-flourish-excel
https://rybicky.net/vyrobky/1741-easylife-easycarbo-rostlinne-hnojivo
https://rybicky.net/vyrobky/2131-co2-vital
https://cs.wikipedia.org/wiki/Glutaraldehyd
http://akvarijni-hnojivo.cz/glutaraldehyd-v-akvaristice-hnojivo-nebo-lakadlo-na-penize-clanek-22
https://rybicky.net/vyrobky/1741-easylife-easycarbo-rostlinne-hnojivo
https://rybicky.net/vyrobky/2131-co2-vital
https://cs.wikipedia.org/wiki/Glutaraldehyd
http://akvarijni-hnojivo.cz/glutaraldehyd-v-akvaristice-hnojivo-nebo-lakadlo-na-penize-clanek-22
Něco o glutaraldehydu jsem sepsal zde. pmdd.mrp-cz.com/…
Budu rád, když to zkritizujete.
Budu rád, když to zkritizujete.
Starší reakce
Dávám cca 10 dní, což je příliš krátká doba na posouzení zda funguje.., nebo se projevuje něco jiného, každopádně od doby co přidávám mi rostlinky bublinkují jak o duši a zrychlil se růst..ovšem došlo i ke změně osvětlení (přidáno), takže to kidně může být světlem 
S timto vyrobkem muzu jenom rict ze rostliny prosperuji a rostou. Kombinuju jeste s Bivojem. Do te doby kytky vubec nerostly. Nic jsem jineho nemenil.
Starší reakce
"Chemicky korektnější" mi přijde spíš takováto formulace: Snížením pH ("okyselením vody") se obsah celkového (anorganického) uhlíku nezvýší, jen se změní poměry jednotlivých složek ve prospěch volného CO2 na úkor (hydrogen)uhličitanů.
Já to vím, hádám se o tom už roky, protože jsem dříve na úpravu pH po výměně vody používal 3% kyselinu solnou. Až ty jsi myslím potvrdil že to tak je. 
Václave :o) ... to už není nic jiného, než slovíčkaření ... ale dobrá ... pokud chceš, tak si všude, kde jsem psal o "zvyšení CO2" dosaď "zvýšení volného CO2" :o))) ... Jinak samozřejmě platí, že když snížím pH, vytěsním z hydrogenuhličitanů kyselinu uhličitou, ta se rozloží na CO2 a vodu (TAKŽE CO2 SE ZVÝŠÍ :o) a CO2 pak utíká pryč z akva, protože je ho zde náhle víc, než kolik odpovídá parciálnímu tlaku CO2 nad hladinou (ale to už se opakuju) ... nic ... venku je pěkně ... jdu s dcerkou na procházku :o) ...
Marcel G napsal: neznám osobně nikoho, kdo by snižoval pH pomocí HCl.
můžeš se zeptat například Václava (resp. vaaclava) :o) ... pokud vím, tak ten s tím má praktické zkušenosti ...
Marcel G napsal: Pokud jde o tvůj poslední komentář, tak já jsem samozřejmě nemluvil o akvárku, kde se bublá z bomby nebo jinak uměle snižuje pH. Zas takový idiot nejsem, abych si něco takového myslel. Mluvil jsem o vodě, kde je ve "výchozím" stavu (tj. po natočení z kohoutku)
Pro tu to samozřejmě platí taky. Vždy to směřuje (tu rychleji, tu pomaleji) k rovnovážnému stavu.
Marcel G napsal: PS: A proč vlastně nám k tomu něco nanapíšeš ty, když jsi chemik?
Páč na to nemám nervy :o) ... Vysvětlovat chemii (na téhle úrovni) ... v internetové "diskusi" ... mám vážné pochybnosti o tom, zda-li je to vůbec možné ... a na vlastní články bohužel stále nemám čas ...
můžeš se zeptat například Václava (resp. vaaclava) :o) ... pokud vím, tak ten s tím má praktické zkušenosti ...
Marcel G napsal: Pokud jde o tvůj poslední komentář, tak já jsem samozřejmě nemluvil o akvárku, kde se bublá z bomby nebo jinak uměle snižuje pH. Zas takový idiot nejsem, abych si něco takového myslel. Mluvil jsem o vodě, kde je ve "výchozím" stavu (tj. po natočení z kohoutku)
Pro tu to samozřejmě platí taky. Vždy to směřuje (tu rychleji, tu pomaleji) k rovnovážnému stavu.
Marcel G napsal: PS: A proč vlastně nám k tomu něco nanapíšeš ty, když jsi chemik?
Páč na to nemám nervy :o) ... Vysvětlovat chemii (na téhle úrovni) ... v internetové "diskusi" ... mám vážné pochybnosti o tom, zda-li je to vůbec možné ... a na vlastní články bohužel stále nemám čas ...
Doma mi stoji ruzne vody a cekam co s tim bude vecer. Uz od pocatku mohu rict, ze drive jsem si byl merenim pH celkem jist, at uz slo o ruzne barevne provedeni pripravku k mereni (papirky ci kapky), aspon +/-0.5, ze bych rozhodne vic neujel, spis min. Ted na to koukam v rozpacich (po tom co tady vsechno slo) a jist si nejsem zda ten odstin vubec prirazuji spravne. Podotykam, ze barvocit mam O.K.
Po trech hodinach je bromthymolova modr v destilce jedlou sodou dotazenou na dKH=4, volne na vzduchu, stale modra, mozna dokonce jeste modrejsi nez hned kdyz jsem to nalil z lahve, kde mam vodu 4dKH namichanou, lahvicka modri nova, byla cerstve otevrena.
Pokud vezmu barvy zde:
www.prirodni-akvarium.cz/…
pak ma minimalne pH=8. To jsme ale cekali. Proste to uhnulo s pH na takovou uroven, kolik je tam parcialni tlak CO2 v atmosfere za danych podminek schopen nacpat (teplota kolem 20°C). Nakonec proto taky funguje dropchecker.
Po trech hodinach je bromthymolova modr v destilce jedlou sodou dotazenou na dKH=4, volne na vzduchu, stale modra, mozna dokonce jeste modrejsi nez hned kdyz jsem to nalil z lahve, kde mam vodu 4dKH namichanou, lahvicka modri nova, byla cerstve otevrena.
Pokud vezmu barvy zde:
www.prirodni-akvarium.cz/…
pak ma minimalne pH=8. To jsme ale cekali. Proste to uhnulo s pH na takovou uroven, kolik je tam parcialni tlak CO2 v atmosfere za danych podminek schopen nacpat (teplota kolem 20°C). Nakonec proto taky funguje dropchecker.
cituji: Akvarista.cz
Od SIDONIUS pro VACLAV
Snížením pH ("okyselením vody") se obsah CO2 nezvýší, jen se změní jeho poměry ve prospěch volného oproti vázanému (obvykle v hydrouhličitanech). Obsah CO2 se zvýší skutečně jen rozkladem organické hmoty, resp. jeho umělým přidáváním v plynné formě.
Od SIDONIUS pro VACLAV
Snížením pH ("okyselením vody") se obsah CO2 nezvýší, jen se změní jeho poměry ve prospěch volného oproti vázanému (obvykle v hydrouhličitanech). Obsah CO2 se zvýší skutečně jen rozkladem organické hmoty, resp. jeho umělým přidáváním v plynné formě.
Předně, nemám problém uznat svůj omyl v některých věcech, co jsem ohledně CO2 psal. Na druhou stranu to, co píšu na svém webu o chemii CO2, jsem konzultoval s vedoucím katedry chemie na fakultě, kde pracuji. Nevidím tedy důvod, proč bych nemohl psát o chemii, i když nejsem vystudovaný chemik. Nicméně uznávám, že v posledním odstavci to tam vysvětluju trochu nešťastně, když jsem psal: Někteří akvaristé se totiž zcela mylně domnívají, že pokud dostatečně sníží hodnotu pH (např. pod 6.0), jakýmsi zázračným způsobem se jim veškerý uhlík přítomný ve vodě přemění z HCO3 na CO2. Nepředpokládal jsem, že by to někdo aplikoval na HCl (neznám osobně nikoho, kdo by snižoval pH pomocí HCl).
Pokud jde o tvůj poslední komentář, tak já jsem samozřejmě nemluvil o akvárku, kde se bublá z bomby nebo jinak uměle snižuje pH. Zas takový idiot nejsem, abych si něco takového myslel. Mluvil jsem o vodě, kde je ve "výchozím" stavu (tj. po natočení z kohoutku) vyšší koncentrace CO2 (např. 7-10 mg/L) ... jak to popisoval Designer. Ten uváděl, že jeho voda z kohoutku má KH 5 a pH 7.3 (= 7.1 mg/L CO2 dle Tillmanovy tabulky). Co mě osobně není jasné, je, zda bude i z téhle vody CO2 utíkat, když rovnovážný stav je někde kolem 0.5 mg/L. To je celé. Každopádně až budu mít více času, zkusím si to lépe nastudovat, abych pak neplácal nesmysly.
PS: A proč vlastně nám k tomu něco nanapíšeš ty, když jsi chemik? Jde nám přece o pochopení toho, jak to funguje. Obzvlášť, když spousta věcí, které tu řešíme, v literatuře není, nebo bys musel opravdu do hloubky studovat chemii, abych dobře chápal všechny vztahy, které tam hrají roli. Pro většinu lidí je obtížné pochopit chemismus vody, když nemají po ruce nikoho, kdo by jim vysvětlil jejich dotazy.
Pokud jde o tvůj poslední komentář, tak já jsem samozřejmě nemluvil o akvárku, kde se bublá z bomby nebo jinak uměle snižuje pH. Zas takový idiot nejsem, abych si něco takového myslel. Mluvil jsem o vodě, kde je ve "výchozím" stavu (tj. po natočení z kohoutku) vyšší koncentrace CO2 (např. 7-10 mg/L) ... jak to popisoval Designer. Ten uváděl, že jeho voda z kohoutku má KH 5 a pH 7.3 (= 7.1 mg/L CO2 dle Tillmanovy tabulky). Co mě osobně není jasné, je, zda bude i z téhle vody CO2 utíkat, když rovnovážný stav je někde kolem 0.5 mg/L. To je celé. Každopádně až budu mít více času, zkusím si to lépe nastudovat, abych pak neplácal nesmysly.
PS: A proč vlastně nám k tomu něco nanapíšeš ty, když jsi chemik? Jde nám přece o pochopení toho, jak to funguje. Obzvlášť, když spousta věcí, které tu řešíme, v literatuře není, nebo bys musel opravdu do hloubky studovat chemii, abych dobře chápal všechny vztahy, které tam hrají roli. Pro většinu lidí je obtížné pochopit chemismus vody, když nemají po ruce nikoho, kdo by jim vysvětlil jejich dotazy.
Vyzkoušejte
Marcel G napsal: No, přiznávám, že nejsem chemik a musím říct, že některé věci mi také nejsou úplně jasné.
No ... já to tak nějak tušil. Ale i tak jsi mě dostal ... Nejsi chemik, ale přesto píšeš články o akvaristcké chemii? Nemyslíš si, že bys měl mít chemii dokonale v malíku a teprve pak ji aplikovat na akvárium? (Abys nedopadl jako Rataj ... ten si taky myslel, jak chemii krásně rozumí ... a vyšly mu z toho neuvěřitelné bláboly ...)
ad "přírodní uzavřený systém" ... a to je čo? Podle mě je to protimluv. Příroda nezná uzavřené systémy. (Jednou ze základních vlastností ekosystému je výměna hmoty a energie s okolím).
ad formy uhlíku - nechápu, proč mi tady vysvětluješ takové triviálnosti (nechemik ... chemikovi :o) to mi hlava nebere
Marcel G napsal: Horác tady mluvil o přidávání silné kyseliny (HCl). ... i když nechápu, proč by někdo něco takového dělal/riskoval)
Snažil jsem se ti vysvětlit, že tvé tvrzení, že snížením pH NELZE zvýšit množství CO2 není pravdivé. To ale neznamená, že bych to tu někomu doporučoval. Přidání silné kyseliny (jak je patrné z mnou uvedených rovnic) snižuje množství hydrogenuhličitanů a tím ovlivňuje pufrační kapacitu vody, což je celkem ošemetná a od určitých hodnot dokonce nebezpečná záležitost.
Marcel G napsal: Pokud jde o přesnou koncentraci CO2 v akvarijní vodě, a o to, zda koncentrace rozpuštěného CO2 ve vodě bude na stále stejné úrovni (podle Tillmanovy tabulky), tak v tom úplně jasno nemám. Musel bych nad tím ještě přemýšlet. Je proto pro mě otázkou, jestli si bude vodovodní voda udržovat stabilní úroveň CO2 na základě vztahu alkality (KH) a pH, nebo jestli se bude koncentrace CO2 ve vodě "přizpůsobovat" rovnovážnému stavu (voda vs. vzduch)
Kristepane ... a co sis myslel? Ať už to céóčko navýšíš (oproti rovnovážnému stavu) jakýmkoliv způsobem (bubláním z bomby nebo snížením pH), ten plyn bude z toho systému unikat. Nebo snad pro akvárium neplatí Henryho zákon?
Fakt si to pořádně nastuduj ... uvědomuješ si vůbec, jaké tu můžeš natropit škody? (byť v dobrém úmyslu?)
No ... já to tak nějak tušil. Ale i tak jsi mě dostal ... Nejsi chemik, ale přesto píšeš články o akvaristcké chemii? Nemyslíš si, že bys měl mít chemii dokonale v malíku a teprve pak ji aplikovat na akvárium? (Abys nedopadl jako Rataj ... ten si taky myslel, jak chemii krásně rozumí ... a vyšly mu z toho neuvěřitelné bláboly ...)
ad "přírodní uzavřený systém" ... a to je čo? Podle mě je to protimluv. Příroda nezná uzavřené systémy. (Jednou ze základních vlastností ekosystému je výměna hmoty a energie s okolím).
ad formy uhlíku - nechápu, proč mi tady vysvětluješ takové triviálnosti (nechemik ... chemikovi :o) to mi hlava nebere
Marcel G napsal: Horác tady mluvil o přidávání silné kyseliny (HCl). ... i když nechápu, proč by někdo něco takového dělal/riskoval)
Snažil jsem se ti vysvětlit, že tvé tvrzení, že snížením pH NELZE zvýšit množství CO2 není pravdivé. To ale neznamená, že bych to tu někomu doporučoval. Přidání silné kyseliny (jak je patrné z mnou uvedených rovnic) snižuje množství hydrogenuhličitanů a tím ovlivňuje pufrační kapacitu vody, což je celkem ošemetná a od určitých hodnot dokonce nebezpečná záležitost.
Marcel G napsal: Pokud jde o přesnou koncentraci CO2 v akvarijní vodě, a o to, zda koncentrace rozpuštěného CO2 ve vodě bude na stále stejné úrovni (podle Tillmanovy tabulky), tak v tom úplně jasno nemám. Musel bych nad tím ještě přemýšlet. Je proto pro mě otázkou, jestli si bude vodovodní voda udržovat stabilní úroveň CO2 na základě vztahu alkality (KH) a pH, nebo jestli se bude koncentrace CO2 ve vodě "přizpůsobovat" rovnovážnému stavu (voda vs. vzduch)
Kristepane ... a co sis myslel? Ať už to céóčko navýšíš (oproti rovnovážnému stavu) jakýmkoliv způsobem (bubláním z bomby nebo snížením pH), ten plyn bude z toho systému unikat. Nebo snad pro akvárium neplatí Henryho zákon?
Fakt si to pořádně nastuduj ... uvědomuješ si vůbec, jaké tu můžeš natropit škody? (byť v dobrém úmyslu?)
Ono to asi nakonec nebude ani potreba, ale i tak diky za ochotu. Staci si uvedomit tohle:
en.wikipedia.org/…
jak vypada ta barva pri neutralnim pH, tedy 7. Je zelena. Nad 7.6 uplne zmodra.
Ja si hral s BEN TEST pH, ktery meri do pH 7.4, a modry byt uplne neumi, je to proste nejaka smeska, at to i cervena pri nizsich pH.
www.krmivajanty.cz/…
Uz mam i bromthymolovou modr, takze si zkusim nechat napln do dropcheckeru den na vzduchu, predpokladam ze uplne zmodra a zustane tak. Zatim jsem totiz nechavat to den volne na vzduchu nemel duvod .
.
en.wikipedia.org/…
jak vypada ta barva pri neutralnim pH, tedy 7. Je zelena. Nad 7.6 uplne zmodra.
Ja si hral s BEN TEST pH, ktery meri do pH 7.4, a modry byt uplne neumi, je to proste nejaka smeska, at to i cervena pri nizsich pH.
www.krmivajanty.cz/…
Uz mam i bromthymolovou modr, takze si zkusim nechat napln do dropcheckeru den na vzduchu, predpokladam ze uplne zmodra a zustane tak. Zatim jsem totiz nechavat to den volne na vzduchu nemel duvod
Já mám docela kvalitní pH metr s dataloggerem (tj. možností ukládání dat), ale momentálně jsme s rodinou v "režimu stěhování", takže je to všechno v některé z cca 50-ti krabic 
Co na to jit z druhe strany:
en.wikipedia.org/…
Solubility in water 1.45 g/L at 25 °C, 100 kPa
CO2 parcialni tlak v atmosfere 40Pa => ve vode 0,58mg/l.
To by tak nejak sedelo k tomu co se uvadi a neresme ted pH a dKH, at se hned nezamotame.
Uzavru system, takze mam dropchecker, ten ma v sobe vzduch s parcialnim tlakem CO2 odpovidajicim obsahu CO2 ve vode (beru to, co funguje). A protoze pridavanim CO2 jej zvysim, pohnu tim difuzi z akvarijni vody do vzduchu v dropchecekeru a nasledne v jeho vode s pH, takze mi ukazuje tim merenim pH (barvou) kolik mam CO2 ve vode, vlastne jakym parcialnim tlakem na vodu v dropcheckeru pusobi a kolik ho tim do ni prejde.
Zmenit moc pH vody v akvariu jen vzdusnym CO2 nejde, protoze koncentrace CO2 ve vzduchu je hodne nizka a take az tak moc nekolisa. Pri rozumnem dkH to treba obycejnym pH papirkem tezko zmerime, nejake zmeny. Vezmu-li domenku, ze pH vody v akvariu bez pridavani CO2 neni zpusobeno onim CO2, ale jen mirne ovlivneno, pak mohu mit vodu s dkH=5, pH=7 a pritom v ni mam CO2 jen 0.5mg/l (plus minus autobus).
Vysledne tedy zbyva zmerit destilku s dotazenim na 4dkH, jake ma pH na vzduchu nejakym presnejsim zpusobem. Pokud ma pH pres 8 (CO2 okolo 0.5mg/l), pak je vsechno O.K. a rikame tim, ze to co dela v akvariu (a i to co tece z kohoutku) pH one vody, neni rozpustene CO2, ale neco jineho, kdyz pri stejnem dKH nema taktez pH pres 8.
Mate prosim nekdo presne meridlo ke zmereni pH v destilce dotazene na dKH=4 a udelate to pro mne, ze to zmerite po dni odstati na vzduchu?
en.wikipedia.org/…
Solubility in water 1.45 g/L at 25 °C, 100 kPa
CO2 parcialni tlak v atmosfere 40Pa => ve vode 0,58mg/l.
To by tak nejak sedelo k tomu co se uvadi a neresme ted pH a dKH, at se hned nezamotame.
Uzavru system, takze mam dropchecker, ten ma v sobe vzduch s parcialnim tlakem CO2 odpovidajicim obsahu CO2 ve vode (beru to, co funguje). A protoze pridavanim CO2 jej zvysim, pohnu tim difuzi z akvarijni vody do vzduchu v dropchecekeru a nasledne v jeho vode s pH, takze mi ukazuje tim merenim pH (barvou) kolik mam CO2 ve vode, vlastne jakym parcialnim tlakem na vodu v dropcheckeru pusobi a kolik ho tim do ni prejde.
Zmenit moc pH vody v akvariu jen vzdusnym CO2 nejde, protoze koncentrace CO2 ve vzduchu je hodne nizka a take az tak moc nekolisa. Pri rozumnem dkH to treba obycejnym pH papirkem tezko zmerime, nejake zmeny. Vezmu-li domenku, ze pH vody v akvariu bez pridavani CO2 neni zpusobeno onim CO2, ale jen mirne ovlivneno, pak mohu mit vodu s dkH=5, pH=7 a pritom v ni mam CO2 jen 0.5mg/l (plus minus autobus).
Vysledne tedy zbyva zmerit destilku s dotazenim na 4dkH, jake ma pH na vzduchu nejakym presnejsim zpusobem. Pokud ma pH pres 8 (CO2 okolo 0.5mg/l), pak je vsechno O.K. a rikame tim, ze to co dela v akvariu (a i to co tece z kohoutku) pH one vody, neni rozpustene CO2, ale neco jineho, kdyz pri stejnem dKH nema taktez pH pres 8.
Mate prosim nekdo presne meridlo ke zmereni pH v destilce dotazene na dKH=4 a udelate to pro mne, ze to zmerite po dni odstati na vzduchu?
No, přiznávám, že nejsem chemik a musím říct, že některé věci mi také nejsou úplně jasné. Ale jak tomu rozumím já, tak Tillmanova tabulka platí především v přírodních uzavřených systémech (kam akvária nepočítám). Tím netvrdím, že to nemůže platit i v některých akváriích, ale primárně se ta tabulka týká přírodních uzavřených systémů. V těchto systémech je uhlík ve vodě obsažen ve 3 formách: 1) CO2 (molekulární oxid uhličitý) a částečně i jako kyselina uhličitá (H2CO3), 2) HCO3 (hydrogenuhličitan), a 3) uhličitan (CO3). Přičemž to, jaká forma uhlíku ve vodě převažuje, závisí na pH. Takže ve vodě s vysokým pH nebude skoro žádný CO2, ale bude tam hodně HCO3/CO3. Naopak ve vodě s nízkým pH bude převládat CO2 na úkor HCO3/CO3. Zároveň bych řekl, že většina povrchových vod u nás bude mít spíše vyšší pH (7-9), a tím pádem v nich nebude tolik uhlíku ve formě CO2, ale spíše ve formě HCO3. [Tak např. ve vodě s pH 8 už není prakticky žádný uhlík ve formě CO2, ale skoro všechen je ve formě HCO3.]
Jiná věc pak je, když si tuto vodu napustíme do nádrže (akvárka), a různě ji dále chemicky upravujeme (jedlá soda, vápenec, CO2 apod.). Tím její rovnováhu uměle vychylujeme. Horác tady mluvil o přidávání silné kyseliny (HCl). Silné kyseliny se ve vodě téměř kompletně rozloží (disociují), což pak může výrazně ovlivnit původní vlastnosti vody. Podle mě ale jakýkoli umělý zásah do původních vlastností vody není žádoucí, a voda se bude mít tendenci se k těm původním hodnotám vracet (pokud nepoužijeme nějaké drastické metody - např. přidání většího množství HCl, i když nechápu, proč by někdo něco takového dělal/riskoval). Podobně se vlastnosti vody budou měnit i přidáváním CO2, neboť určitá (malá) část CO2 se ve vodě rozloží (disociuje) na slabou kyselinu (H2CO3), která vlastnosti vody také určitou (malou) měrou změní - tj. sníží mírně pH (obvykle tak o 0.5 až 1 stupeň). Jakmile ale s umělým přidáváním CO2 přestaneme, voda se začne vracet k původním vlastnostem (hodnotám) ... pokud jsme ji tedy nepřipravili o její soli a další látky. Změna vlastností vody (především pH) v důsledku přidávání CO2 bude tedy jen dočasná.
Pokud jde o přesnou koncentraci CO2 v akvarijní vodě, a o to, zda koncentrace rozpuštěného CO2 ve vodě bude na stále stejné úrovni (podle Tillmanovy tabulky), tak v tom úplně jasno nemám. Musel bych nad tím ještě přemýšlet. Je proto pro mě otázkou, jestli si bude vodovodní voda udržovat stabilní úroveň CO2 na základě vztahu alkality (KH) a pH, nebo jestli se bude koncentrace CO2 ve vodě "přizpůsobovat" rovnovážnému stavu (voda vs. vzduch) až na úroveň kolem 1 mg/L. Tohle jsem si zatím nijak neověřoval, a ani teoreticky o tom moc nevím. Co ale vím, je, že když budu vydatně čeřit vodní hladinu v akváriu (a přísun CO2 bude zastavený), tak mi koncentrace CO2 klesne až na cca 1-2 mg/L. V mém případě to ale může být právě ta "původní" hodnota, kterou moje voda měla, když jsem ji natočil z kohoutku. Možná, že když bude mít někdo výchozí hodnotu 7 mg/L CO2, tak se ani vydatným čeřením hladiny pod tuto původní hodnotu nedostane (o čemž ale trochu pochybuji, protože vydatným promícháváním vody se vzduchem [= čeřením], se voda bude mít tendenci všech plynů zbavovat). To, že mi tedy těch 7 mg/L CO2 nebude z vody neunikat, bude možná proto, že bude jeho "únik" velmi pozvolný (hlavně díky absenci pořádného promíchávání vody a vzduchu).
Jiná věc pak je, když si tuto vodu napustíme do nádrže (akvárka), a různě ji dále chemicky upravujeme (jedlá soda, vápenec, CO2 apod.). Tím její rovnováhu uměle vychylujeme. Horác tady mluvil o přidávání silné kyseliny (HCl). Silné kyseliny se ve vodě téměř kompletně rozloží (disociují), což pak může výrazně ovlivnit původní vlastnosti vody. Podle mě ale jakýkoli umělý zásah do původních vlastností vody není žádoucí, a voda se bude mít tendenci se k těm původním hodnotám vracet (pokud nepoužijeme nějaké drastické metody - např. přidání většího množství HCl, i když nechápu, proč by někdo něco takového dělal/riskoval). Podobně se vlastnosti vody budou měnit i přidáváním CO2, neboť určitá (malá) část CO2 se ve vodě rozloží (disociuje) na slabou kyselinu (H2CO3), která vlastnosti vody také určitou (malou) měrou změní - tj. sníží mírně pH (obvykle tak o 0.5 až 1 stupeň). Jakmile ale s umělým přidáváním CO2 přestaneme, voda se začne vracet k původním vlastnostem (hodnotám) ... pokud jsme ji tedy nepřipravili o její soli a další látky. Změna vlastností vody (především pH) v důsledku přidávání CO2 bude tedy jen dočasná.
Pokud jde o přesnou koncentraci CO2 v akvarijní vodě, a o to, zda koncentrace rozpuštěného CO2 ve vodě bude na stále stejné úrovni (podle Tillmanovy tabulky), tak v tom úplně jasno nemám. Musel bych nad tím ještě přemýšlet. Je proto pro mě otázkou, jestli si bude vodovodní voda udržovat stabilní úroveň CO2 na základě vztahu alkality (KH) a pH, nebo jestli se bude koncentrace CO2 ve vodě "přizpůsobovat" rovnovážnému stavu (voda vs. vzduch) až na úroveň kolem 1 mg/L. Tohle jsem si zatím nijak neověřoval, a ani teoreticky o tom moc nevím. Co ale vím, je, že když budu vydatně čeřit vodní hladinu v akváriu (a přísun CO2 bude zastavený), tak mi koncentrace CO2 klesne až na cca 1-2 mg/L. V mém případě to ale může být právě ta "původní" hodnota, kterou moje voda měla, když jsem ji natočil z kohoutku. Možná, že když bude mít někdo výchozí hodnotu 7 mg/L CO2, tak se ani vydatným čeřením hladiny pod tuto původní hodnotu nedostane (o čemž ale trochu pochybuji, protože vydatným promícháváním vody se vzduchem [= čeřením], se voda bude mít tendenci všech plynů zbavovat). To, že mi tedy těch 7 mg/L CO2 nebude z vody neunikat, bude možná proto, že bude jeho "únik" velmi pozvolný (hlavně díky absenci pořádného promíchávání vody a vzduchu).
Designer napsal: Tim chces rict, ze Tillmanova tabulka plati jen pro vodu uzavrenou v bedne bez pristupu atmosfery?
Přesně tak. Množství CO2 totiž není dáno pouze hodnotou pH (viz Henderson-Hasselbachova rovnice), ale také parciálním tlakem CO2 nad vodní hladinou ... Tím se právě liší uzavřený systém od otevřeného (akvárium). To je to, oč mi šlo ... Snížením pH (přidáním silné kyseliny) mohu zvýšit množství CO2 v akváriu (a ne že ne) ... takto vzniklý CO2 mi ovšem uteče, protože jeho množství je větší, než odpovídá zmíněnému parc. tlaku ...
Přesně tak. Množství CO2 totiž není dáno pouze hodnotou pH (viz Henderson-Hasselbachova rovnice), ale také parciálním tlakem CO2 nad vodní hladinou ... Tím se právě liší uzavřený systém od otevřeného (akvárium). To je to, oč mi šlo ... Snížením pH (přidáním silné kyseliny) mohu zvýšit množství CO2 v akváriu (a ne že ne) ... takto vzniklý CO2 mi ovšem uteče, protože jeho množství je větší, než odpovídá zmíněnému parc. tlaku ...
Chtělo by to šikovného chemika, jinak se tu budeme motat v kruhu.
Já si naopak myslím, že jakmile se nejedná o čistou vodu, ale vodu, kde je rozpouštěný vápník a hydrogenuhličitany, tak je rovnovážná koncentrace CO2 mnohem vyšší.
Já si naopak myslím, že jakmile se nejedná o čistou vodu, ale vodu, kde je rozpouštěný vápník a hydrogenuhličitany, tak je rovnovážná koncentrace CO2 mnohem vyšší.
Tim chces rict, ze Tillmanova tabulka plati jen pro vodu uzavrenou v bedne bez pristupu atmosfery?
Protoze pokud ne, pak bych natocil nejakou vodu, nechal ji odstat, a zmerim v ni po odstati pH vyssi, protoze unikne CO2. A nejen ze by to pH bylo pri CO2 0.5mg/l vysoke, ono by bylo pri me uhlicitanove tvrdosti 5dKH uz mimo rozsah bezne uvadenych udaju, tedy zmeritelne ruzne snad cimkoli.
A nerikal tady nekdo, ze vodarny vodovodni vodu zbavuji CO2, aby jim nerezavely trubky vlivem nizkeho pH?
A mam gualse 2 .
.
Protoze pokud ne, pak bych natocil nejakou vodu, nechal ji odstat, a zmerim v ni po odstati pH vyssi, protoze unikne CO2. A nejen ze by to pH bylo pri CO2 0.5mg/l vysoke, ono by bylo pri me uhlicitanove tvrdosti 5dKH uz mimo rozsah bezne uvadenych udaju, tedy zmeritelne ruzne snad cimkoli.
A nerikal tady nekdo, ze vodarny vodovodni vodu zbavuji CO2, aby jim nerezavely trubky vlivem nizkeho pH?
A mam gualse 2
Johan napsal: A není koncentrace rozpuštěného CO2 cca 0,5 mg/l v destilce? 
Myslím, že taková bude nakonec v každé vodě - viz planta.aquariana.cz/… . Samozřejmě v některých vodách může být přirozená koncentrace CO2 vyšší, v jiných nižší. Rovnovážný stav ale zůstane vždy stejný, nicméně do některých vod je pak CO2 dotováno z jiných zdrojů - např. z podloží, nebo rozkládajících se organických látek.
Myslím, že taková bude nakonec v každé vodě - viz planta.aquariana.cz/… . Samozřejmě v některých vodách může být přirozená koncentrace CO2 vyšší, v jiných nižší. Rovnovážný stav ale zůstane vždy stejný, nicméně do některých vod je pak CO2 dotováno z jiných zdrojů - např. z podloží, nebo rozkládajících se organických látek.
Koncentrace 0.5 mg/L CO2 je tzv. rovnovážný stav, který nastane, až se hladina CO2 ve vodě (tj. tvých výchozích 7.1 mg/L) vyrovná s hladinou CO2 ve vzduchu. Jinými slovy, pokud máš ve vodě vyšší koncentraci CO2 než je ve vzduchu, tak ti bude CO2 z vody pomalinku utíkat, a to tak dlouho, až se jeho koncentrace ve vodě vyrovná s koncentrací ve vzduchu - tj. až se ve vodě ustálí na těch cca 0.5 mg/L. No, ono to není tak úplně přímočaré, protože rovnávážný stav bude nastávat především tam, kde bude voda přicházet do styku se vzduchem (tedy především u vodní hladiny). Pokud by ti voda v akvárku stála a vodní hladina se nehýbala, bude k vyrovnávání rozdílných koncentrací docházet asi velmi pomalu. Když se ti ale bude voda v akvárku točit a budeš navíc hodně čeřit hladinu, bude se to k rovnávážnému stavu blížit rychleji. Já třeba přidávám do akvárka asi 30 mg/L CO2, a když přísun CO2 vypnu, koncentrace se mi vrací do výchozí hodnoty relativně pomalu, a nikdy mi během noci nekleslo pod cca 10 mg/L. Když ale přitom začnu hodně čeřit hladinu, vyprchá mi CO2 z vody mnohem rychleji, takže už za pár hodin jsem díky čeření na koncentraci 1-2 mg/L CO2.
Přirovnal bych to tak trochu ke dvěma místnostem s rozdílnými teplotami. Akvárko je pokoj s teplotou 20st.C, zatímco vzduch je místnost s teplotou 1st.C. A jak asi každý ví, udržet v akvárku teplotu 20st.C, když je venku 1st.C, dlouho nepůjde, pokud nebudeš to svoje akvárko trochu přihřívat (= uměle dodávat CO2, které ti z něj bude neustále unikat).
Přirovnal bych to tak trochu ke dvěma místnostem s rozdílnými teplotami. Akvárko je pokoj s teplotou 20st.C, zatímco vzduch je místnost s teplotou 1st.C. A jak asi každý ví, udržet v akvárku teplotu 20st.C, když je venku 1st.C, dlouho nepůjde, pokud nebudeš to svoje akvárko trochu přihřívat (= uměle dodávat CO2, které ti z něj bude neustále unikat).
A není koncentrace rozpuštěného CO2 cca 0,5 mg/l v destilce? 
No super, dostavame se kam jsem chtel, konecne se zbavim stareho gulase (a to nejsem hostinskej)  .
.
Takze Tillmanova tabulka rika kH 5 - pH 7.3 = 7.1mg/l CO2.
Ty pises:
Jak známo, přirozená (rovnovážná) hladina rozpuštěného CO2 ve vodě se pohybuje kolem 0.5 mg/L.
Ano, ten udaj taky znam, take jsem s nim nedavno operoval. Ale ted kde je ten zakopany pes?
Jasne, pH vody neni ovliveno jen tim CO2, muzu jej posunout i jinak, ale berme idelani pripad, nebo alespon ze zhruba plati.
Takze Tillmanova tabulka rika kH 5 - pH 7.3 = 7.1mg/l CO2.
Ty pises:
Jak známo, přirozená (rovnovážná) hladina rozpuštěného CO2 ve vodě se pohybuje kolem 0.5 mg/L.
Ano, ten udaj taky znam, take jsem s nim nedavno operoval. Ale ted kde je ten zakopany pes?
Jasne, pH vody neni ovliveno jen tim CO2, muzu jej posunout i jinak, ale berme idelani pripad, nebo alespon ze zhruba plati.
Přiznám se, že teď nějak nemám kapacitu na to, abych si ověřil, jestli je správný údaj, že 0.4 mg/L glutaraldehydu odpovídá 0.8 mg/L CO2. I tak bych ale řekl, že tvůj předpoklad o "udržení" stabilní koncentrace CO2 v akváriu na hodnotě kolem 7-8 mg/L pomocí čeření hladiny (nebo vzduchování) asi nebude správný. Jak známo, přirozená (rovnovážná) hladina rozpuštěného CO2 ve vodě se pohybuje kolem 0.5 mg/L. Takže pokud budeš vydatně čeřit vodní hladinu (a nebude ti ve vodě vznikat žádné další CO2), tak ti bude díky čeření hladiny tato koncentrace možná pomalu, ale neustále klesat, dokud se nedosáhne rovnovážného stavu. K tomu můžeš připočíst i fakt, že nějakou část toho CO2 ti budou z vody odčerpávat i rostliny, takže podle mě nelze udržet trvale stejnou koncentraci CO2 ve vodě bez toho, abys tam nějaké to CO2 dodával (buď častější výměnou vody, se kterou bys tam nějaké to CO2 zase dostal ... nebo umělým přidáváním zvenčí). Dokud budeš mít ve vodě koncentraci CO2 vyšší než 0.5 mg/L, tak ti bude čeření hladiny jeho koncentraci neustále srážet (směrem k této rovnovážné hodnotě).
PS: Vliv čeření hladiny a vzduchování na koncentraci CO2 jsem si ověřoval, a zjistil jsem, že vzduchování nemá na koncentraci CO2 téměř žádný vliv (pravděpodobně proto, že bublinky vzduchu jsou příliš velké, příliš rychle uniknou k hladině, a na vodní masu jich je v akváriu příliš málo). Čeření hladiny je v tomto ohledu mnohem účinnější.
PS: Vliv čeření hladiny a vzduchování na koncentraci CO2 jsem si ověřoval, a zjistil jsem, že vzduchování nemá na koncentraci CO2 téměř žádný vliv (pravděpodobně proto, že bublinky vzduchu jsou příliš velké, příliš rychle uniknou k hladině, a na vodní masu jich je v akváriu příliš málo). Čeření hladiny je v tomto ohledu mnohem účinnější.
Kdyz tady mam tu moznost, i o tom co bezne cekat od kohoutku se samozrejme rad dozvim vic nez mohu zjistit volne na webu, takze dik i za tohle info z praxe  .
.
Pokud vezmeme tyto realne hodnoty, a rekneme ze mam uvedenych kH 5 - pH 7.3 = 7.1mg/l CO2 (5dKH jsem nameril, pH muze tak nejak taky podle mereni sedet, na desetinky tim co mam to nezmerim).
A kdyz se podivam niz, co pise Marcel:
Marcel G napsal: Z jejich měření je ale také patrné, že největší "skok" se odehrává mezi koncentrací 1 mg/L a 7 mg/L (nárůst o 300%). Rozdíl v růstu mezi koncentrací 7 mg/L a 35 mg/L už je při nízkém až středním osvětlení velmi malý. Díky tomu bych řekl, že většině akvaristů by mělo stačit maximálně 10 mg/L CO2. Větší množství už nemá na růst rostlin větší vliv (tzn. přidáváme-li více než 10 mg/L, nezískáme tím už prakticky žádný podstatný nárůst rostlinné biomasy).
zjistuji, ze svych 7.1mg/l CO2 mam, takze bych s tim mohl byt nejak spokojen i jak to je, staci mi dostatecne cerit hladinu k dostatecne difuzi, nebo poradne vzduchovat, pro doplneni CO2 ze vzduchu, k doplneni jeho spotreby (4 male rybicky me 200l akvarium ohledne CO2 nevytrhnou). Je samozrejme mozne, ze uvedeny udaj z uvedeneho mereni muze mit ruznou verohodnost, pisu o situaci, ze tomu udaji budu verit, z pohledu ciste teorie. Nebudu-li tedy chtit zavodit o kazdou desetinku gramu na prirustcich rostlin, pridavani CO2 se mohu vzdat a nemusim si z toho delat tezkou hlavu.
A ted se konecne dostavam okruhem i ke glutaradehydu, kam jsem se chtel puvodne dostat, ale pak to uz moc odbocilo a nemel jsem ty spravne teoreticke argumenty po ruce. Glutaraldehyd obsahuje okolo 60% uhliku, CO2 jej obsahuje 27.29% (hmotnostne), rekneme polovinu. Pokud by rostliny byly schopny spotrebovavat glutaraldehyd stejne jako CO2 (klidne ho tak berme, vypoctu to neublizi at je to jakkoli), at uz ho spotrebuji kolik chteji, je jeho koncentrace 0.4mg/l asi takova, jako bych zvysil obsah CO2 o 0.8mg/l, tedy ze svych 7.1mg/l na 7.9mg/l (tedy pokud se mi podari jen co nejlepsi difuzi vzduchu do vody tuto hladinu udrzet). A to myslim mohu povazovat za dosti bezvyznamnou zmenu, nez abych lil rybam do vody toxickou latku, byt v male a rekneme nezavadne koncentraci.

Pokud vezmeme tyto realne hodnoty, a rekneme ze mam uvedenych kH 5 - pH 7.3 = 7.1mg/l CO2 (5dKH jsem nameril, pH muze tak nejak taky podle mereni sedet, na desetinky tim co mam to nezmerim).
A kdyz se podivam niz, co pise Marcel:
Marcel G napsal: Z jejich měření je ale také patrné, že největší "skok" se odehrává mezi koncentrací 1 mg/L a 7 mg/L (nárůst o 300%). Rozdíl v růstu mezi koncentrací 7 mg/L a 35 mg/L už je při nízkém až středním osvětlení velmi malý. Díky tomu bych řekl, že většině akvaristů by mělo stačit maximálně 10 mg/L CO2. Větší množství už nemá na růst rostlin větší vliv (tzn. přidáváme-li více než 10 mg/L, nezískáme tím už prakticky žádný podstatný nárůst rostlinné biomasy).
zjistuji, ze svych 7.1mg/l CO2 mam, takze bych s tim mohl byt nejak spokojen i jak to je, staci mi dostatecne cerit hladinu k dostatecne difuzi, nebo poradne vzduchovat, pro doplneni CO2 ze vzduchu, k doplneni jeho spotreby (4 male rybicky me 200l akvarium ohledne CO2 nevytrhnou). Je samozrejme mozne, ze uvedeny udaj z uvedeneho mereni muze mit ruznou verohodnost, pisu o situaci, ze tomu udaji budu verit, z pohledu ciste teorie. Nebudu-li tedy chtit zavodit o kazdou desetinku gramu na prirustcich rostlin, pridavani CO2 se mohu vzdat a nemusim si z toho delat tezkou hlavu.
A ted se konecne dostavam okruhem i ke glutaradehydu, kam jsem se chtel puvodne dostat, ale pak to uz moc odbocilo a nemel jsem ty spravne teoreticke argumenty po ruce. Glutaraldehyd obsahuje okolo 60% uhliku, CO2 jej obsahuje 27.29% (hmotnostne), rekneme polovinu. Pokud by rostliny byly schopny spotrebovavat glutaraldehyd stejne jako CO2 (klidne ho tak berme, vypoctu to neublizi at je to jakkoli), at uz ho spotrebuji kolik chteji, je jeho koncentrace 0.4mg/l asi takova, jako bych zvysil obsah CO2 o 0.8mg/l, tedy ze svych 7.1mg/l na 7.9mg/l (tedy pokud se mi podari jen co nejlepsi difuzi vzduchu do vody tuto hladinu udrzet). A to myslim mohu povazovat za dosti bezvyznamnou zmenu, nez abych lil rybam do vody toxickou latku, byt v male a rekneme nezavadne koncentraci.
Oba příklady které uvádíš mají příliš velký obsah CO2 taková voda ti z kohoutku nepoteče.
Spíše by to mohlo vypadat takhle.
kH 5 - pH 7,3 = 7,1mg/l CO2
kH 8 - pH 7,6 = 5,7mg/l CO2

Spíše by to mohlo vypadat takhle.
kH 5 - pH 7,3 = 7,1mg/l CO2
kH 8 - pH 7,6 = 5,7mg/l CO2
No dyk prave, sice nepouzivam kalkulator, ale koukam do Tillmanovy tabulky, coz je predpokladam totez co vyplivne kalkulator. Tu predstavu o vzajemnem vztahu uhlicitanove tvrdosti a pH k obsahu CO2 ve vode mam.
Kdyz pridam CO2, snizi se pH.
Cim mam vyssi uhlicitanovou tvrdost, tim mene pH hybu dolu pri pridani stejne koncentrace CO2 do vody.
Cim mam vyssi uhlicitanovou tvrdost a nizsi pH, tim vice CO2 voda obsahuje.
A kdyz mam stejne pH, voda s vyssi uhlicitanovou tvrdosti obsahuje vice CO2.
Abych stahnul pH vody na stejnou uroven, rekneme ze 7 na 6.5, musim pri vyssi uhlicitanove tvrdosti vic bublat CO2, ale tim budu mit ve vode take CO2 vice. Takze pokud chci dosahnout stejne koncentrace CO2 ve vode (ne stejneho snizeni pH), pri vyssi uhlicitanove tvrdosti nemusim tolik pridavat, protoze uz tam vic CO2 je.
Prikladem:
Mam vodu s uhlicitanovou tvrdosti 5 a pH=7. V tabulce vidim CO2 15mg/l.
Nekdo jiny ma 8dKH a pH=7. V tabulce vidim CO2 26mg/l.
Pokud bych chtel dotahnout CO2 na uroven 40mg/l, v prvnim pripade musim pribublat 25mg/l, ve druhem jen 14mg/l, pri vyssi uhlicitanove tvrdosti mene.
A ano, docetl jsem se i to, ze pH ovlivnuji i dalsi veci nez CO2 (ale tak to vime obecne snad vsichni), ktere se tehle tabulce vymykaji a pak se neda pouzit. Nicmene v idelanim pripade (nic neni idealni, souhlas), musim pri stejnem pH a vyssi uhlicitanove tvrdosti dodat do vody mene CO2, abych dosahl stejnou koncentraci.
Radeji to uz popisuji az takhle, at uz se dozvim, kde delam tu zatracenou chybu .
.
Kdyz pridam CO2, snizi se pH.
Cim mam vyssi uhlicitanovou tvrdost, tim mene pH hybu dolu pri pridani stejne koncentrace CO2 do vody.
Cim mam vyssi uhlicitanovou tvrdost a nizsi pH, tim vice CO2 voda obsahuje.
A kdyz mam stejne pH, voda s vyssi uhlicitanovou tvrdosti obsahuje vice CO2.
Abych stahnul pH vody na stejnou uroven, rekneme ze 7 na 6.5, musim pri vyssi uhlicitanove tvrdosti vic bublat CO2, ale tim budu mit ve vode take CO2 vice. Takze pokud chci dosahnout stejne koncentrace CO2 ve vode (ne stejneho snizeni pH), pri vyssi uhlicitanove tvrdosti nemusim tolik pridavat, protoze uz tam vic CO2 je.
Prikladem:
Mam vodu s uhlicitanovou tvrdosti 5 a pH=7. V tabulce vidim CO2 15mg/l.
Nekdo jiny ma 8dKH a pH=7. V tabulce vidim CO2 26mg/l.
Pokud bych chtel dotahnout CO2 na uroven 40mg/l, v prvnim pripade musim pribublat 25mg/l, ve druhem jen 14mg/l, pri vyssi uhlicitanove tvrdosti mene.
A ano, docetl jsem se i to, ze pH ovlivnuji i dalsi veci nez CO2 (ale tak to vime obecne snad vsichni), ktere se tehle tabulce vymykaji a pak se neda pouzit. Nicmene v idelanim pripade (nic neni idealni, souhlas), musim pri stejnem pH a vyssi uhlicitanove tvrdosti dodat do vody mene CO2, abych dosahl stejnou koncentraci.
Radeji to uz popisuji az takhle, at uz se dozvim, kde delam tu zatracenou chybu
Stáhni si kalkulátor CO2 a můžeš si to skoušet, aby jsi měl představu jak to funguje. 
Vyzkoušejte
Já už se v tomn tady taky ztracen  založil jsem téma CO2 Vital - zkušenosti a najednou se tu píše o chemických reakcích a až pomalu vědeckých debatách
založil jsem téma CO2 Vital - zkušenosti a najednou se tu píše o chemických reakcích a až pomalu vědeckých debatách 
Marcel G napsal: Takže podle mého měkká voda obsahuje ve výchozím stavu (tj. bez uměle přidávaného CO2) obvykle mnohem více oxidu uhličitého než tvrdá voda...
A to asi chapu spatne . Destilka prirozene nepojme ohledne CO2 skoro nic, voda s 5dKH mnohem vic, rekneme klidne 40x tolik pri stejne teplote a stejnem pH. Ten rozdil je propastny. Chapu ze voda s vyssi uhlicitanovou tvrdosti bude mit v podstate automaticky i vyssi pH ve stavu jak je, ale stale mi to nesedi.
. Destilka prirozene nepojme ohledne CO2 skoro nic, voda s 5dKH mnohem vic, rekneme klidne 40x tolik pri stejne teplote a stejnem pH. Ten rozdil je propastny. Chapu ze voda s vyssi uhlicitanovou tvrdosti bude mit v podstate automaticky i vyssi pH ve stavu jak je, ale stale mi to nesedi.
Mam v tom proste gulas, a ne proto ze nectu, ze se nesnazim, asi jsem na tohle blbej...
A to asi chapu spatne
Mam v tom proste gulas, a ne proto ze nectu, ze se nesnazim, asi jsem na tohle blbej...
Já myslím, že to píšeš (chápeš) správně.
1) Čím nižší pH (a vyšší KH), tím více přirozeného CO2 budeš ve vodě mít. Takže zde platí, že voda o pH třeba 6.5 bude obsahovat více CO2 než voda s pH 8 (desetiny až jednotky vs. desítky až stovky mg/L CO2 v závislosti na KH). Takže do vody, která má nízké pH, už logicky není potřeba přidávat tolik (nebo vůbec žádné) CO2 => viz Tillmanova tabulka. Tohle je to, o čem jsem psal v souvislosti s "výchozí" (přirozenou) koncentrací CO2.
2) Něco jiného je ale "rozpustnost" uměle přidávaného CO2 v měkké vs. tvrdé vodě. Zde si myslím, že žádný rozdíl není. To znamená, že pokud budu do vody přidávat třeba 5 b/s CO2, tak mi to koncentraci oxidu uhličitého zvýší naprosto stejně, ať už to budu přidávat do měkké nebo tvrdé vody. Ovšem v součtu budu mít samozřejmě více CO2 v měkké vodě, protože ta už sama o sobě obsahovala mnohem větší výchozí množství CO2 než tvrdá voda s vysokým pH.
Takže podle mého měkká voda obsahuje ve výchozím stavu (tj. bez uměle přidávaného CO2) obvykle mnohem více oxidu uhličitého než tvrdá voda, ale pokud jde o uměle přidávané CO2, tak to se bude v měkké vodě rozpouštět úplně stejně jako v tvrdé vodě (tj. když přidám do měkké vody 10 mg/L CO2, budu ho tam mít 10 mg/L; když přidám stejné množství do tvrdé vody, budu ho tam mít stejně => pomineme-li teď ty výchozí hodnoty, které byly ve vodě před přidáváním CO2). Pokud bych chtěl tedy ušetřit něco málo peněz za CO2 z tlakové láhve, tak je samozřejmě lepší používat měkčí vodu (s nižším pH), kde už bude ve výchozím stavu vyšší koncentrace CO2. Takovou pak mohu dotovat přidaným CO2 v mnohem menší míře (nebo vůbec). Pokud ale vím, tak většina vodáren produkuje pitnou vodu s pH kolem 7-8, ve které tolik "přirozeného" CO2 není.
1) Čím nižší pH (a vyšší KH), tím více přirozeného CO2 budeš ve vodě mít. Takže zde platí, že voda o pH třeba 6.5 bude obsahovat více CO2 než voda s pH 8 (desetiny až jednotky vs. desítky až stovky mg/L CO2 v závislosti na KH). Takže do vody, která má nízké pH, už logicky není potřeba přidávat tolik (nebo vůbec žádné) CO2 => viz Tillmanova tabulka. Tohle je to, o čem jsem psal v souvislosti s "výchozí" (přirozenou) koncentrací CO2.
2) Něco jiného je ale "rozpustnost" uměle přidávaného CO2 v měkké vs. tvrdé vodě. Zde si myslím, že žádný rozdíl není. To znamená, že pokud budu do vody přidávat třeba 5 b/s CO2, tak mi to koncentraci oxidu uhličitého zvýší naprosto stejně, ať už to budu přidávat do měkké nebo tvrdé vody. Ovšem v součtu budu mít samozřejmě více CO2 v měkké vodě, protože ta už sama o sobě obsahovala mnohem větší výchozí množství CO2 než tvrdá voda s vysokým pH.
Takže podle mého měkká voda obsahuje ve výchozím stavu (tj. bez uměle přidávaného CO2) obvykle mnohem více oxidu uhličitého než tvrdá voda, ale pokud jde o uměle přidávané CO2, tak to se bude v měkké vodě rozpouštět úplně stejně jako v tvrdé vodě (tj. když přidám do měkké vody 10 mg/L CO2, budu ho tam mít 10 mg/L; když přidám stejné množství do tvrdé vody, budu ho tam mít stejně => pomineme-li teď ty výchozí hodnoty, které byly ve vodě před přidáváním CO2). Pokud bych chtěl tedy ušetřit něco málo peněz za CO2 z tlakové láhve, tak je samozřejmě lepší používat měkčí vodu (s nižším pH), kde už bude ve výchozím stavu vyšší koncentrace CO2. Takovou pak mohu dotovat přidaným CO2 v mnohem menší míře (nebo vůbec). Pokud ale vím, tak většina vodáren produkuje pitnou vodu s pH kolem 7-8, ve které tolik "přirozeného" CO2 není.
No vzniklo to cele, ta debata, vlastne timhle (alespon si to myslim):
vaaclav napsal: Spotřeba Co2 závisí na tom jakou máš uhličitanovou tvrdost(dkH). Čím tvrdší voda tím více musíš bublat a naopak.
A kdyz se podivam na Tillmanovu tabulku, pri vyssi uhlicitanove tvrdosti mam CO2 ve vode vic (obecne, jasne ze pH neni jen o obsahu CO2, to je mi jasne). Takze abych dosahl stejne koncentrace CO2 ve vode (ne stejne nizkeho pH), mel bych prece budblat mene (vice jen pokud chci dosahnout stejne nizkeho pH, ale slo o stejnou koncentraci CO2, ne o stejne pH). A dropchecker ma klasicky destilku s doplnenou uhlicitanovou tvrdosti na rovno 4, nepracuje s vodou v akvariu, ale jen s plyny v akvarijni vode, bude tedy ukazovat koncentraci CO2 stejne, at mam v akvariu uhlicitanovou tvrdost jekoukoli, tedy pokud jedu podle nej, mel bych se dostavat na stejne mnozstvi CO2, jeho stejene pH, stejnou koncetraci CO2, ne na stejne pH vody v akvariu). Takze dochazim k opacnemu zaveru, ze ve vode s vyssi uhlicitanovou tvrdosti mi staci bublat mene, abych dosahl stejne koncentrace CO2, protoze ta voda uz prirozene nejake CO2 pojme ve vetsi mire, nez kdyby tu uhlicitanovou tvrdost mela nizsi. Pokud by se ovsem co pridavam ohledne CO2 do vody nedostavalo hure, coz je to, co netusim a co se snazil popsat Marcel, ze to bude stejne.
Pokud budu bublat CO2 v akvarijni vode a budu merit primo jeji pH, samozrejme ze na pH=6.5 se dostanu s vyssi uhlicitanovou tvrdosti az po pridani vice CO2, ta vyssi uhlicitanova tvrdost mi to snizeni pH pomoci CO2 tak snadno neumozni. Ze rostlinam vyhovuje lepe nizsi pH, budiz, ale kvuli tomu ze mam uhlicitanovou tvrdost dejme tomu 10 (mam 5, ale to je tady vedlejsi), nebudu prece hnat koncentraci CO2 v akvariu na 100mg/l jen proto, abych dosahl v akvariu pH=6.5.
Mozna jsou me zavery mylne, ale snad od toho tady ta debata je, abych si je i ja dal dohromady. Ale tak snad to vsichni zname, kazdy jsme z nejakeho oboru a i kdyz si neco precteme, snazime si to dat dohromady, nejsme v tom uplne doma a zaver muze byt spatny. Takze mne prosim nebijte, ptam se na to, s cim mam v hlave problem .
.
vaaclav napsal: Spotřeba Co2 závisí na tom jakou máš uhličitanovou tvrdost(dkH). Čím tvrdší voda tím více musíš bublat a naopak.
A kdyz se podivam na Tillmanovu tabulku, pri vyssi uhlicitanove tvrdosti mam CO2 ve vode vic (obecne, jasne ze pH neni jen o obsahu CO2, to je mi jasne). Takze abych dosahl stejne koncentrace CO2 ve vode (ne stejne nizkeho pH), mel bych prece budblat mene (vice jen pokud chci dosahnout stejne nizkeho pH, ale slo o stejnou koncentraci CO2, ne o stejne pH). A dropchecker ma klasicky destilku s doplnenou uhlicitanovou tvrdosti na rovno 4, nepracuje s vodou v akvariu, ale jen s plyny v akvarijni vode, bude tedy ukazovat koncentraci CO2 stejne, at mam v akvariu uhlicitanovou tvrdost jekoukoli, tedy pokud jedu podle nej, mel bych se dostavat na stejne mnozstvi CO2, jeho stejene pH, stejnou koncetraci CO2, ne na stejne pH vody v akvariu). Takze dochazim k opacnemu zaveru, ze ve vode s vyssi uhlicitanovou tvrdosti mi staci bublat mene, abych dosahl stejne koncentrace CO2, protoze ta voda uz prirozene nejake CO2 pojme ve vetsi mire, nez kdyby tu uhlicitanovou tvrdost mela nizsi. Pokud by se ovsem co pridavam ohledne CO2 do vody nedostavalo hure, coz je to, co netusim a co se snazil popsat Marcel, ze to bude stejne.
Pokud budu bublat CO2 v akvarijni vode a budu merit primo jeji pH, samozrejme ze na pH=6.5 se dostanu s vyssi uhlicitanovou tvrdosti az po pridani vice CO2, ta vyssi uhlicitanova tvrdost mi to snizeni pH pomoci CO2 tak snadno neumozni. Ze rostlinam vyhovuje lepe nizsi pH, budiz, ale kvuli tomu ze mam uhlicitanovou tvrdost dejme tomu 10 (mam 5, ale to je tady vedlejsi), nebudu prece hnat koncentraci CO2 v akvariu na 100mg/l jen proto, abych dosahl v akvariu pH=6.5.
Mozna jsou me zavery mylne, ale snad od toho tady ta debata je, abych si je i ja dal dohromady. Ale tak snad to vsichni zname, kazdy jsme z nejakeho oboru a i kdyz si neco precteme, snazime si to dat dohromady, nejsme v tom uplne doma a zaver muze byt spatny. Takze mne prosim nebijte, ptam se na to, s cim mam v hlave problem
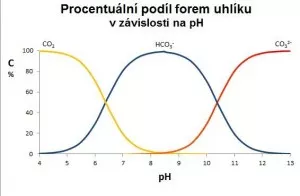 Jakmile odeberete CO2, snížíte jeho poměr vůči HCO3-, takže pohnete s pH (směrem nahoru). Přidáte li CO2, opět vychýlíte jeho poměr vůči HCO3-, takže pohnete s pH (směrem dolů). Jednoduchý princip. Můžete si to ověřit a zkonstruovat si graf vztahů jednotlivých fotem uhličitanového systému pomocí Henderson-Hasselbachových rovnic.
Jakmile odeberete CO2, snížíte jeho poměr vůči HCO3-, takže pohnete s pH (směrem nahoru). Přidáte li CO2, opět vychýlíte jeho poměr vůči HCO3-, takže pohnete s pH (směrem dolů). Jednoduchý princip. Můžete si to ověřit a zkonstruovat si graf vztahů jednotlivých fotem uhličitanového systému pomocí Henderson-Hasselbachových rovnic. Ovšem k Tillmanově tabulce se nevyjadřuji, protože nevím, co vlastně má ukazovat.
HCl + NaHCO3 = H2CO3 + NaCl (rovnováha reakce posunutá velmi silně doprava)
H2CO3 = H2O + CO2 (rovnováha reakce opět posunutá velmi silně doprava)
Tohle prostě platí a tys to ve svém článku (a ve svém příspěvku v 18:20) popřel (Napsals, že je to blbost). A já s tím nesouhlasím. Toť vše.
O přidávání CO2 a jeho vlivu na pH jsem já nenapsal ani slovo.
H2CO3 = H2O + CO2 (rovnováha reakce opět posunutá velmi silně doprava)
Tohle prostě platí a tys to ve svém článku (a ve svém příspěvku v 18:20) popřel (Napsals, že je to blbost). A já s tím nesouhlasím. Toť vše.
O přidávání CO2 a jeho vlivu na pH jsem já nenapsal ani slovo.
Marcel G napsal: PS: Jen připomínám, že se zde stále bavíme o rozdílu KH v důsledku umělého přidávání CO2 (nikoli v důsledku přidávání HCl).
Nikoliv. Přesně naopak. Já se (od samého počátku) bavím právě jen a pouze o zvýšení množství CO2 po přidání HCl :o))) ... O ničem jiném.
Nikoliv. Přesně naopak. Já se (od samého počátku) bavím právě jen a pouze o zvýšení množství CO2 po přidání HCl :o))) ... O ničem jiném.
Přiznám se, že moc nerozumím tomu, v čem zde vidíš problém. Podle tebe ten článek popírá elementární chemické zákony. V čem přesně? Vždyť v tom článku je to, co jsem zde v kostce shrnul ... a to (jak sám uvádíš) nezpochybňuješ. V čem je tedy problém nebo nesrovnalost? Já zde přece nikde nemluvím o přidávání většího množství HCl, ale pouze o přidávání CO2, jehož MALÁ ČÁST reaguje s vodou za vzniku [malého množství] H2CO3. Možná jsem natvrdlý, ale nějak mi uniká pointa tvé námitky. Jde přece o to, že kyselina, která vzniká při reakci CO2 s vodou, je v natolik malém množství, že na celkovou [přirozenou] koncentraci CO2 ve vodě nebude mít prakticky žádný [měřitelný] vliv. To samozřejmě neznamená, že nebude mít vůbec žádný vliv (tj. že by zde neplatily fyzikální zákony, které popisuješ), ale pro naše účely je tento vliv naprosto zanedbatelný. To si konec konců můžeš sám ověřit tím, že budeš měřit alkalitu v akváriu, do kterého budeš uměle přidávat CO2. Pokud se ti povede naměřit nějaký významnější rozdíl v alkalitě, tak klobouk dolů. PS: Jen připomínám, že se zde stále bavíme o rozdílu KH v důsledku umělého přidávání CO2 (nikoli v důsledku přidávání HCl).
Vyzkoušejte
Ten článek jsem četl (a podle mě popírá elementární chemické zákony - alespoň ty, které se učí na VŠChT v Praze a na farmacii v Hradci Králové :o). (Ony se vlastně učí už na základní škole :o). Přečti si lépe můj příspěvek. Já nezpochybňuju to, co jsi teď popsal (tj. relativně malý vliv přidaného CO2 na pokles pH)... já jsem zpochybnil to, že přídavek silné kyseliny (samozřejmě po vyčerpání pufrační kapacity vody) nezvyšuje množství CO2 (jde o triviální reakci vytěsnění slabé kyseliny kyselinou silnější, přičemž tato slabší kyselina se následně rozpadá).
Nevím, jestli jsi se díval na ten článek, na který odkazuji, ale pokud vím (a ověřoval jsem si to i u chemiků), tak pouze MALÁ ČÁST uměle přidávaného CO2 (jen asi 0.2-1%) reaguje s vodou za vzniku kyseliny uhličité (H2CO3), a z ní pak opět pouze MALÁ ČÁST dále disociuje na HCO3- a H+. Takže ani relativně velký nárůst CO2 nevyvolá významný pokles pH (obvykle dojde k poklesu pH tak maximálně o 1 stupeň). Takže toto nepatrné množství hydrogenuhličitanu (HCO3) nebude mít žádný měřitelný vliv na hodnotu KH (alkalitu). Myslím si, že ohledně tohoto tématu panuje mezi akvaristy hodně mylných představ a málokdo se obtěžuje si ty věci nějak ověřovat.
Takže ano, silná kyselina sice alkalitu snižuje, ale v případě umělého přidávání CO2 je této kyseliny (H2CO3) tak malé a zanedbatelné množství, že to na alkalitu žádný praktický vliv mít nebude.
Takže ano, silná kyselina sice alkalitu snižuje, ale v případě umělého přidávání CO2 je této kyseliny (H2CO3) tak malé a zanedbatelné množství, že to na alkalitu žádný praktický vliv mít nebude.
Já bych řekl že to jestli mám tvrdou nebo měkkou vodu z alkalitou dost souvisí hlavně v případě že třeba na noc přísun CO2 přeruším.
Jak si změříš nebo spočítáš obsah CO2 když neplatí u umělého sycení tilmanova tabulka např. 30mg/l.
Jak si změříš nebo spočítáš obsah CO2 když neplatí u umělého sycení tilmanova tabulka např. 30mg/l.
Blbost? Neplatí snad, že se přidáváním silné kyseliny snižuje alkalita? Neplatí snad, že silnější kyselina (např. HCl) vytěsňuje slabší kyselinu (uhličitou) z její soli (uhličitan, hydrogenuhličitan)? A neplatí snad, že kyselina uhličitá je natolik nestálá, že se (téměř za 100%) rozpadá na volný oxid uhličitý a vodu?
Designer napsal: Musim vic bublat, abych dosahl ne stejneho pH vody, ale stejne koncentrace CO2 ve vode pri vyssi uhlicitanove tvrdosti? Dostava se CO2 do vody hure pri vyssi uhlicitanove tvrdosti?
To si nemyslím. Tillmanova tabulka ukazuje, kolik CO2 je ve výchozím stavu v přírodních vodách (tj. uzavřených systémech), které nemají s umělým přidáváním CO2 co do činění. V takových systémech závisí obsah CO2 na alkalitě. Někteří akvaristé se ale na základě toho mylně domnívají, že když pak ve svém akvárku snížím uměle pH nebo KH, automaticky se tím ve vodě "objeví" více nebo méně CO2 ... což je blbost. Pokud budu do vody cpát 35 mg/L CO2, budu tam mít 35 mg/L CO2 ... ať už bude ta voda tvrdá nebo měkká. Alkalita (uhličitanová tvrdost) určuje přirozený obsah CO2. Pokud mám tvrdou vodu a nízké pH, pak budu mít ve výchozím stavu ve vodě vysoký obsah CO2. Například při pH 6 a KH 1 to bude 30 mg/L CO2. Pokud ale budu do takové vody přidávat 15 mg/L CO2, tak se mi výchozí koncentrace CO2 zvýší právě o těch přidaných 15 mg/L CO2. To samé ale bude platit u tvrdé vody. Tzn. že pokud budu mít tvrdou vodu (pH 8 a KH 10), bude moje výchozí koncentrace CO2 jen 3 mg/L. Když ale budu do vody přidávat 15 mg/L CO2 z tlakové lahve, tak se mi výchozí koncentrace CO2 (v tomto případě 3 mg/L) zvýší opět o 15 mg/L. Uměle přidané CO2 tedy s alkalitou vody příliš nesouvisí, a toto CO2 se rozpustí naprosto stejně v měkké i v tvrdé vodě. Rozdíl je jen v tom, že pokud mám měkkou vodu (= nízké pH), tak není třeba přidávat do vody moc CO2 ... protože ho v takové vodě už bude pravděpodobně dost samo o sobě (i bez umělého přidávání z tlakové lahve).
Mám k tomu článek i na svých stránkách: prirodni-akvarium.cz/… .
To si nemyslím. Tillmanova tabulka ukazuje, kolik CO2 je ve výchozím stavu v přírodních vodách (tj. uzavřených systémech), které nemají s umělým přidáváním CO2 co do činění. V takových systémech závisí obsah CO2 na alkalitě. Někteří akvaristé se ale na základě toho mylně domnívají, že když pak ve svém akvárku snížím uměle pH nebo KH, automaticky se tím ve vodě "objeví" více nebo méně CO2 ... což je blbost. Pokud budu do vody cpát 35 mg/L CO2, budu tam mít 35 mg/L CO2 ... ať už bude ta voda tvrdá nebo měkká. Alkalita (uhličitanová tvrdost) určuje přirozený obsah CO2. Pokud mám tvrdou vodu a nízké pH, pak budu mít ve výchozím stavu ve vodě vysoký obsah CO2. Například při pH 6 a KH 1 to bude 30 mg/L CO2. Pokud ale budu do takové vody přidávat 15 mg/L CO2, tak se mi výchozí koncentrace CO2 zvýší právě o těch přidaných 15 mg/L CO2. To samé ale bude platit u tvrdé vody. Tzn. že pokud budu mít tvrdou vodu (pH 8 a KH 10), bude moje výchozí koncentrace CO2 jen 3 mg/L. Když ale budu do vody přidávat 15 mg/L CO2 z tlakové lahve, tak se mi výchozí koncentrace CO2 (v tomto případě 3 mg/L) zvýší opět o 15 mg/L. Uměle přidané CO2 tedy s alkalitou vody příliš nesouvisí, a toto CO2 se rozpustí naprosto stejně v měkké i v tvrdé vodě. Rozdíl je jen v tom, že pokud mám měkkou vodu (= nízké pH), tak není třeba přidávat do vody moc CO2 ... protože ho v takové vodě už bude pravděpodobně dost samo o sobě (i bez umělého přidávání z tlakové lahve).
Mám k tomu článek i na svých stránkách: prirodni-akvarium.cz/… .
maniakva.sweb.cz/…
Pokud tomu nerozumíš tak si z odkazu přečti jak to funguje.
Dnes se to obchází i tím že se všechno CO2 ve vodě nerozpustí ale pomocí například atomizérů se z něho vytváří mlha, kterou silný proud prožene celým akváriem a bublinky se buď rozpustí, nebo ulpívají na listech. Předpokládám že je rostliny dokáží nějak využít.
Pokud tomu nerozumíš tak si z odkazu přečti jak to funguje.
Dnes se to obchází i tím že se všechno CO2 ve vodě nerozpustí ale pomocí například atomizérů se z něho vytváří mlha, kterou silný proud prožene celým akváriem a bublinky se buď rozpustí, nebo ulpívají na listech. Předpokládám že je rostliny dokáží nějak využít.
Cim bude vyssi uhlicitanova tvrdost, tim vice musim dostat do vody CO2, abych dosahl stejne pH, rekneme abych z pH 7 udelal 6.5 (prikladem, podle Tillmanovy tabulky, to je jasne). Ale musim i vic bublat, abych dosahl ne stejneho pH vody, ale stejne koncentrace CO2 ve vode pri vyssi uhlicitanove tvrdosti? Dostava se CO2 do vody hure pri vyssi uhlicitanove tvrdosti?
Spotřeba Co2 závisí na tom jakou máš uhličitanovou tvrdost(dkH). Čím tvrdší voda tím více musíš bublat a naopak.
Nikdy jsem nehloubal nad tím kolik ho rostliny spotřebují ale jednoznačně jsem si vyzkoušel že 20 - 40mg/l funguje velmi dobře. Doporučené koncentrace se v čase stále zvětšují, od nějakých 12mg/l až po už zmíněných 50mg/l.
Co2 není jen zdrojem uhlíku, ale také okyseluje vodu a dostat se pod Ph 7 (neutrální) má své další výhody a to při malých koncentrací moc nejde. Pro většinu rostlin a ryb je nižší Ph přirozenější.
Nikdy jsem nehloubal nad tím kolik ho rostliny spotřebují ale jednoznačně jsem si vyzkoušel že 20 - 40mg/l funguje velmi dobře. Doporučené koncentrace se v čase stále zvětšují, od nějakých 12mg/l až po už zmíněných 50mg/l.
Co2 není jen zdrojem uhlíku, ale také okyseluje vodu a dostat se pod Ph 7 (neutrální) má své další výhody a to při malých koncentrací moc nejde. Pro většinu rostlin a ryb je nižší Ph přirozenější.
Tohle jsem nemyslel, ale rohodne je to dobra vec pro alespon nejakou predstavu, diky  .
.
Udělal jsem na to na svých stránkách jednoduchou kalkulačku: www.prirodni-akvarium.cz/… . Ale nejsem si jistý, jestli myslíš přesně tohle.
To jiste, samozrejme ze samotne CO2 nic neresi a rostliny si vezmou jen co mohou s ohledem na vsechno dalsi. A vlastne i to samotne udrzeni koncentrace bude zavisle na dalsich parametrech vody, jeji teplotou pocinaje, konce obsahem vseho mozneho. Prilis jsem to zjednodusil, uznavam.
EDIT: Jinak mi neslo o CO2 "kolik stoji" v penezich, ale ve smyslu jeho spotreby. Ono poridit si malou lahev a litat pak kazdou chvili plnit jiste neni nic moc, ale zase skladovat doma neco zbytecne velkeho... A pokud by platilo, co napsal Marcel, ze koncentrace CO2 nad 10mg/l je celkem zbytecna, mozna by proti udrzovani zminenych 35mg/l mohla stacit lahev mensi nez je obvykle, ktera se lepe vejde mezi "smeti" ve stojanu.
EDIT: Jinak mi neslo o CO2 "kolik stoji" v penezich, ale ve smyslu jeho spotreby. Ono poridit si malou lahev a litat pak kazdou chvili plnit jiste neni nic moc, ale zase skladovat doma neco zbytecne velkeho... A pokud by platilo, co napsal Marcel, ze koncentrace CO2 nad 10mg/l je celkem zbytecna, mozna by proti udrzovani zminenych 35mg/l mohla stacit lahev mensi nez je obvykle, ktera se lepe vejde mezi "smeti" ve stojanu.
Spotřeba CO2 není závislá na udržení nějaké její koncentrace ale na tom jakou máš vodu. Kdyby bylo všechno tak laciné jako CO2 tak to bych si pořídil ještě jednu nádrž. 
https://rybicky.net/vyrobky/1534-flourish-excel
https://rybicky.net/vyrobky/1741-easylife-easycarbo-rostlinne-hnojivo
https://rybicky.net/vyrobky/2131-co2-vital
https://cs.wikipedia.org/wiki/Glutaraldehyd
http://akvarijni-hnojivo.cz/glutaraldehyd-v-akvaristice-hnojivo-nebo-lakadlo-na-penize-clanek-22
https://rybicky.net/vyrobky/1741-easylife-easycarbo-rostlinne-hnojivo
https://rybicky.net/vyrobky/2131-co2-vital
https://cs.wikipedia.org/wiki/Glutaraldehyd
http://akvarijni-hnojivo.cz/glutaraldehyd-v-akvaristice-hnojivo-nebo-lakadlo-na-penize-clanek-22
Zpět na obsah sekce CO2 • Zobrazeno 8103x
Máte připomínku nebo nápad? Napište nám vzkaz do redakce nebo s námi diskutujte.
